Corona-Themen in der Übersicht

zum Artikel

zum Artikel
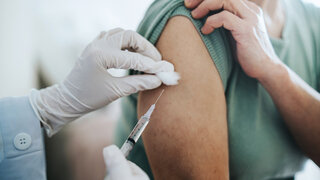
zum Artikel

zum Artikel

zum Artikel

zum Artikel
zum Artikel
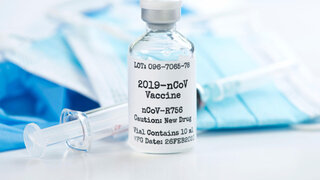
zum Artikel
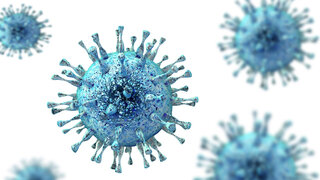
zum Artikel

zum Artikel

zum Artikel

zum Artikel

zum Artikel
zum Artikel

zum Artikel
Coronavirus bei Kindern und Schwangeren

zum Artikel

zum Artikel

zum Artikel
Diabetes und Coronavirus
zum Artikel

zum Artikel
zum Artikel