Multiples Myelom / Plasmozytom
Was ist ein Multiples Myelom?
Bei dieser Erkrankung breitet sich ein Klon (genetisch identische Zellen) von entarteten Plasmazellen (Myelomzellen) im Knochenmark aus. Plasmazellen allgemein gehören zur Gruppe der B-Lymphozyten, welche in der Lage sind, Antikörper (Immunglobuline) zu produzieren. Beim Multiplen Myelom vermehrt sich eine Plasmazelle, welche funktionslose Antikörper produziert. Häufig befallen die entarteten Plasmazellen verschiedene Stellen des Skeletts gleichzeitig. Bei dieser diffusen Infiltration spricht man von einem Multiplen Myelom. Bilden die Myelomzellen einen einzelnen umschriebenen Tumor, welcher auch außerhalb des Knochenmarks auftreten kann (extramedullär), spricht man von einem Plasmozytom. Das Plasmozytom ist damit eine Sonderform des Myeloms.
Das Multiple Myelom wird zur Gruppe der Non-Hodgkin-Lymphome gezählt.
Die Erkrankung ist selten, ist aber die zweithäufigste bösartige Erkrankung des blutbildenden Systems. Die Häufigkeit wird mit drei bis vier neuen Erkrankungsfällen pro 100.000 Einwohner und Jahr in Deutschland (Inzidenz) angegeben. Das durchschnittliche Erkrankungsalter liegt bei Männern bei 72 Jahren, bei Frauen bei 74 Jahren.
Ursachen: Was sind Auslöser für Myelome?
Entartete Plasmazellen führen zu einem Multiplen Myelom. Warum die Plasmazellen entarten, ist aber bisher unklar. Als begünstigende Faktoren werden ionisierende Strahlung, Pestizide und Benzol diskutiert, ebenso wie Fettleibigkeit (Adipositas) und chronische Infektionen. Die Erkrankung kann selten familiär gehäuft auftreten. Bei circa 40 Prozent der Erkrankten findet sich eine genetische Veränderung (Trisomien und Gentranslokationen bestimmter Chromosomen). Dies weist auf eine mögliche erbliche Komponente hin. Als typische Erbkrankheit gilt das Multiple Meylom aber bisher nicht.
Klinische Vorstufen des Multiplen Myeloms sind die Monoklonale Gammopathie unklarer Signifikanz (MGUS) und das schwelende (smouldering) Myelom.
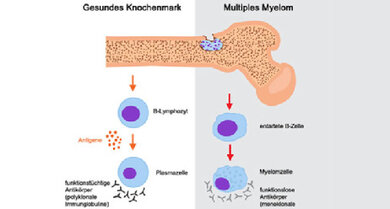
Beim Multiplen Myelom entartet eine Plasmazelle (B-Zell-Lymphozyt)
© Shutterstock/Fancy Tapis

Rückenschmerzen können viele Ursachen haben manchmal steckt ein multiples Myelom dahinter
© Fotolia/Robert Kneschke
Symptome: Welche Beschwerden bereitet ein Multiples Myelom?
- Knochenschmerzen: Die häufigsten Beschwerden beim Multiplen Myelom sind Knochenschmerzen und hier insbesondere Rückenschmerzen durch den Befall der Wirbelsäule. Die Schmerzen nehmen häufig bei Bewegung zu. Ursache sind oft zunächst unbemerkte Knochenbrüche. Bedingt werden diese sogenannten pathologischen Frakturen durch eine Ausdünnung des Knochens durch die Tumorzellen. Da das Multiple Myelom sich von Anfang an in den Knochen ausbreitet, gehören die Symptome des Knochenbefalls zu den eher frühen Beschwerden.
Die Beschwerden können, wenn keine entsprechenden weiteren Untersuchungen durchgeführt werden, zu Beginn auch als Rheuma oder Osteoporose fehlgedeutet werden.
- Blutarmut: Auch eine Blutarmut (Anämie) tritt, zumindest in milder Form, oft schon in frühen Stadien auf. Sie kann durch Blässe (vor allem der Schleimhäute), Müdigkeit, Abgeschlagenheit, Kopfschmerzen und eingeschränkte körperliche Leistungsfähigkeit auffallen aber auch unbemerkt bleiben, vor allem wenn sie sich langsam entwickelt.
- Erhöhte Infektanfälligkeit: Aufgrund der zunehmenden Verdrängung des gesunden Knochenmarks durch die Tumorzellen kommt es zu einer Störung der Blutbildung im Knochenmark mit einer Verminderung von roten und weißen Blutkörperchen. Durch einen Mangel an speziellen weißen Blutkörperchen (Leukopenie), den sogenannten Granulozyten und an normalen B-Zellen (Plasmazellen), die funktionsfähige Antikörper bilden, kommt es zu einer Abwehrschwäche. Die Patienten neigen vermehrt zu Infektionen vor allem bakterieller Art.
- Nierenfunktionsstörung: In späteren Krankheitsstadien können Beschwerden durch eine zunehmende Nierenfunktionsstörung auftreten. Folgen einer Nierenfunktionsstörung sind unter anderem Wassereinlagerungen (Ödeme). Bei einer fortgeschrittenen Nierenschädigung kann die Harnproduktion zunächst vermindert sein (Oligurie) und zuletzt völlig versiegen (Anurie). Mehr zu den Symptomen entnehmen Sie bitte dem Ratgeber Nierenversagen.
- Schäumender Urin: Einige Patienten berichten über einen übermäßig schäumenden Urin. Dies kommt bei Patienten vor, bei denen die Plasmazellen vor allem Leichtketten-Proteine (Bence-Jones-Proteine) bilden, welche vermehrt mit dem Urin ausgeschieden werden. Die Bence-Jones-Proteinurie findet sich aber auch bei anderen Lymphomerkrankungen.
- Verwirrtheit und Muskelkrämpfe: Aufgrund des erhöhten Knochenabbaus, ausgelöst durch die Osteoklastenaktivierung durch Myelomzellen (siehe Infokasten "Welche Folgen hat ein Multiples Myelom?") erhöht sich der Kalziumspiegel im Blut (Hyperkalzämie), was sich in Verwirrtheit und Muskelkrämpfen wiederspiegeln kann.
- Gewichtsverlust: Im Rahmen der Tumorerkrankung kann es zu einem ungewollten Gewichtsverlust kommen.
Des Weiteren können sich folgende Symptome zeigen:
Die vom Tumor gebildeten Immunglobuline können zu einer Eindickung des Blutes führen (Hyperviskositätssyndrom). Es entstehen unter Umständen Durchblutungsstörungen unterschiedlicher Ausprägung – von der schmerzhaften Minderdurchblutung einzelner Finger bis hin zu Durchblutungsstörungen lebenswichtiger Organe (Herzinfarkt, Gehirnschlag, Infarkte an den inneren Organen).
Vergleichsweise selten kommt es auch zu einer Störung in der Bildung von Blutplättchen mit einer Blutungsneigung. Typisch sind hier eine verlängerte Blutungszeit nach einer Verletzung und / oder punktförmige Einblutungen an der Haut (sogenannte Petechien).
In manchen Fällen werden die von den Myelomzellen gebildeten Leichtketten (siehe Infokasten "Was passiert nun bei einem Multiplen Myelom") in Organen wie Herz, Niere, Magen-Darm-Trakt, Leber oder Milz abgelagert (Amyloidose) und können die Funktion der Organe beeinträchtigen. Es kann sogar zu einem vollständigen Funktionsverlust (Nieren- oder Leberinsuffizienz) kommen.

Im Röntgenbild sind viele Myelomherde (schwarze Flecken) zu erkennen
© Shutterstock/Santibhavank P.
Diagnose: Wie stellt der Arzt ein Multiples Myelom fest?
Die Krankheit kann auf unterschiedlichen Wegen entdeckt werden. Bei vielen Patienten führen auffällige Blut- oder Urinbefunde als Zufallsbefund zur Diagnose. Hinweise auf die Erkrankung gibt häufig eine extrem hohe Blutsenkungsgeschwindigkeit oder eine Eiweißerhöhung im Blut oder im Urin. Bei anderen Patienten wird die Erkrankung aufgrund von Knochenschmerzen entdeckt. Bei Verdacht auf ein Multiples Myelom schließen sich verschiedene diagnostische Maßnahmen an.
Neben dem Arztgespäch und der körperlichen Untersuchung sind folgende weitere Untersuchungen zur Diagnosestellung wichtig: eine Knochenmarkpunktion mit zytogenetischen Untersuchungen, Laboruntersuchungen (unter anderem die Eiweißzusammensetzung in Blut und Urin) und radiologische Untersuchungen (Röntgenaufnahmen, CT, MRT, PET) des Skeletts.
Knochenmarkpunktion: Hier wird – unter örtlicher Betäubung – mit Hilfe einer dicken Hohlnadel der Knochen zum Beispiel am oberen Beckenkamm bis zum Markraum durchbohrt und, ähnlich einer Blutentnahme, eine geringe Menge des Knochenmarks angesaugt (aspiriert) oder direkt herausgestanzt (Stanzbiopsie). Das gewonnene Material wird zur weiteren Untersuchung in ein Labor gesandt, die aspirierten Zellen werden unter dem Mikroskop zytologisch untersucht. Die Stanzbiopsie wird ebenfalls unter dem Mikroskop nach speziellen Schnitt- und Färbetechniken histologisch untersucht.
Laboruntersuchungen (Blut- und Urinuntersuchungen):
- Serum-Eiweiß-Elektrophorese und Nachweis von Eiweiß im Urin: Bei einer Serum-Eiweiß-Elektrophorese werden verschiedene Eiweißtypen voneinander getrennt. Bei einem Multiplen Myelom sind große Mengen gleichartiger Eiweißkörper vorhanden. Dabei lassen sich zwei Typen, nämlich das monoklonale Immunglobulin (Paraprotein) und die monoklonalen Leichtkettenproteine unterscheiden. Das monoklonale Immunglobulin ist in der Elektrophorese als schmalbasiger Gipfel zu erkennen (M-Gradient). Die Leichtketten (sogenannte Bence Jones-Proteine) kann man auch im Urin (24-Stunden Sammelurin) nachweisen. Urinteststreifen sind zum Nachweis von Paraprotein nicht geeignet.
Das Beta-2-Mikroglobulin ist ebenfalls ein Eiweiß, welches im Urin und im Blutserum bestimmt wird und ist ein Maß für die Nierenfunktion. - Weitere Blutserumuntersuchungen: Bestimmung des Differenzialblutbildes (rote und weiße Blutkörperchen und Blutplättchen), der Blutsalze (Natrium, Kalium, Kalzium), der Nierenwerte, Entzündungswerte und Parameter der Blutgerinnung.
Bildgebende Verfahren: Um den Krankheitsverdacht weiter zu erhärten und das Krankheitsstadium abschätzen zu können, wird ein sogenannter Röntgen-Skelett-Status erhoben. Früher wurde dies mit Hilfe konventioneller Röntgenaufnahmen nach einem festgelegten Schema durchgeführt (Pariser Schema, beinhaltet Röntgenbilder von Schädel, Wirbelsäule, Rippen, Becken, Oberschenkelknochen und Oberarmknochen). Heutzutage erfolgt aber meist eine sogenannte "low-dose"-Ganzkörper-Computertomographie-Untersuchung. Diese spezielle Form von Computertomografie arbeitet mit einer niedrigen Strahlendosis und gilt als das Verfahren, das auch gering ausgeprägte Auflösungserscheinungen am Knochen (Osteolysen) am genauesten darstellen kann. Eine Magnetresonanztomographie (MRT) kann beispielsweise bei der Beurteilung von Tumoren im Bereich der Wirbelsäule und der Beurteilung von Weichteilanteilen hilfreich sein.

Die Therapie bei multiplem Myelom richtet sich nach dem individuellen Fall. Sie kann zum Beispiel eine Chemotherapie beinhalten
© iStock/Annedde
Therapie: Wie wird ein Multiples Myelom behandelt?
Ziele der Behandlung eines Myeloms sind die Kontrolle der Symptome, das heißt, die Betroffenen sollen möglichst keine Beschwerden haben, sowie eine Lebensverlängerung durch anhaltende Remission. Remission bedeutet in der Medizin, dass die Krankheit nicht mehr nachweisbar ist. Dies ist aber nicht mit einer Heilung gleichzusetzen. Meistens empfiehlt man den Betroffenen, sich im Rahmen von Studien in spezialisierten Zentren behandeln zu lassen. In vielen Fällen ist so eine erfolgreiche Therapie möglich. Da die Erkrankung bei jedem Patienten stark variiert, ist eine individuelle Therapieplanung nötig.
Wer muss behandelt werden?
Ob ein Myelom behandelt werden muss oder nicht, hängt davon ab, ob der Betroffene Beschwerden hat und ob durch die Erkrankung bereits Schäden im Körper vorhanden sind. Zu den Kriterien, die die Notwendigkeit einer Therapie bestimmen gehören die sogenannten CRAB-Kriterien (Hypercalcemia – erhöhter Kalziumspiegel im Blut, renal insufficiency – Niereninsuffizienz, anemia – Blutarmut, bone lesions – Knochenbeteiligung). Ergänzt werden die CRAB-Kriterien durch bildgebende Verfahren und serologischen Untersuchungsparametern. Bereits ein Kriterium reicht für eine Therapienotwendigkeit aus.
Andere Gründe für eine Behandlung sind beispielsweise ein Hyperviskositätssyndrom, oder allgemeine Krankheitszeichen wie Fieber über 38°C ohne erkennbare Ursache, Nachtschweiß oder ungewollter Gewichtsverlust über 10 Prozent in den letzten sechs Monaten (sogenannte B-Symptome) und myelombedingten Schmerzen.
Patienten mit asymptomatischem Myelom müssen in der Regel nicht sofort behandelt werden. Sie sollten engmaschig überwacht werden, so dass bei Beschwerden unverzüglich eine Behandlung eingeleitet werden kann. In klinischen Studien wird untersucht, ob eine frühzeitigere Behandlung den Verlauf der Erkrankung günstig beeinflussen kann. Belegt werden konnte das generell bislang nicht.
Ist eine Therapie angebracht, unterscheidet sich das Vorgehen vor allem nach dem Alter und dem Gesundheitszustand des Betroffenen. Die Behandlung erfolgt nach einem individuellen Behandlungsplan.
Welche Behandlungsmöglichkeiten gibt es?
Als sogenannte Erstlinientherapie erhalten Patienten, welche bei der Erstdiagnose dafür infrage kommen, eine autologe Stammzellentransplantation. Diese intensivierten Therapiekonzepte kommen vorwiegend für jüngere Patienten (biologisches Alter ≤70) in gutem Allgemeinzustand und ohne Begleiterkrankungen zum Einsatz.
Die Erstlinientherapie mit Hochdosistherapie teilt sie dann wie folgt ein:
- Induktion
- Hochdosistherapie mit autologer Transplantation
- Konsolidierung (falls nötig)
- Erhaltung (gegebenenfalls)
Induktionstherapie für Hochdosistherapie: Einen wichtigen Stellenwert in der Therapie haben neben Chemotherapeutika auch sogenannte neue Substanzen wie Bortezomib, Lenalidomid und Thalidomid. Sie verbessern die Wirksamkeit und die Ansprechraten einer klassischen Chemotherapie. Diese positiven Effekte müssen gegen ihre Nebenwirkurgen, und mögliche Spätnebenwirkungen abgewogen werden. Meist werden die Wirkstoffe in Kombination in drei bis vier Zyklen verabreicht. Ziel der Induktionstherapie ist es, die Krankheit gut zu kontrollieren oder gar eine Remission zu erreichen, um gute Ausgangsbedingungen für die Stammzellentransplantation zu haben.
Hochdosistherapie mit autologer Stammzellentransplantation: Der Zeitpunkt der Stammzellensammlung wird in Abhängigkeit vom Ansprechen auf die Induktionstherapie festgelegt. Zur Mobilisierung der Stammzellen wird zunächst ein Wachstumsfaktor (G-CSF; Granulocyten-Kolonie-stimulierender-Faktor) alleine oder in Kombination mit einer Chemotherapie gegeben. Der Wachstumsfaktor bewirkt das Ablösen von Vorläuferzellen aus dem Knochenmark. Diese werden in die Blutbahn freigesetzt und können so entnommen werden (Apharese). Anschließend erfolgt eine hochdosierte Chemotherapie, meist mit Melphalan, um möglichst viele Myelomzellen abzutöten. Bei dieser Behandlung kommt es jedoch gleichzeitig zu einer massiven Unterdrückung des normalen Knochenmarkes. Daher wurden dem Patienten vor der Behandlung die Blutstammzellen entnommen. Diese werden nach Abschluss der Chemotherapie dem Patienten wieder zurückgegeben (transfundiert, autolog=von sich selbst gewonnene Stammzellen).
Zusätzliche Konsolidierungstherapie: Nach erfolgter Stammzellentransplantation kann insbesondere bei Patienten, welche nach der Transplantation (gegebenenfalls auch zwei Transplantationen möglich) keine Remission erreicht haben, eine weiterführende Konsolidierungstherapie sinnvoll sein. Diese besteht zum Beispiel aus den Medikamenten der Induktionstherapie.
Erhaltungstherapie: Auch nach erfolgreicher Behandlung besteht ein hohes Risiko für einen Rückfall. Die neuen Medikamente Bortezomib, Lenalidomid und Thalidomid können mithelfen, einen Rückfall zu verzögern. Eine Erhaltungstherapie mit diesen Wirkstoffen kann sowohl nach intensivierten Therapiekonzepten als auch nach konventioneller Chemotherapie erwogen werden. Bislang ist der Nutzen für alle Patientengruppen noch nicht abschließend geklärt. Zugelassen als Erhaltungstherapie ist in Europa derzeit lediglich Lenalidomid bei Patienten mit Multiplem Myelom nach autologer Stammzellttransplantation (ABSZT). Die Erhaltungstherapie ist nach wie vor Gegenstand klinischer Forschung.
Wenn keine Transplantation möglich ist:
Bei Betroffenen, die älter als 70 Jahre beziehungsweise gebrechlich sind oder zusätzlich zum Multiplen Myelom unter anderen Erkrankungen leiden, wird in der Regel eine konventionelle dosierte Induktionstherapie empfohlen. Dabei können neben Chemotherapeutika auch die neuen Substanzen wie Bortezomib, Lenalidomid und Thalidomid in Kombination mit einem Kortisonpräparat zum Einsatz kommen. Aktuell gibt es zwei zwei Standardtherapien, nämlich VMP (Velcade + Melphalan + Prednisolon) oder Rd (Revlimid/Lenalidomid + Dexamethason).
Wie behandelt man ein Plasmozytom?
Ein Plasmozytom kann man mit gutem Erfolg bestrahlen. Manchmal ist zusätzlich eine Operation notwendig. Etliche Patienten können so geheilt werden. Bei einem Teil der so behandelten Patienten kann sich im Verlauf der nächsten 10 Jahre jedoch auch ein Rezidiv in Form eines Multiplen Myeloms entwickeln.
Ergänzende Therapiemaßnahmen
Einen hohen Stellenwert in der Behandlung des Multiplen Myeloms haben unterstützende Maßnahmen. Bisphosphonate können dem Verlust von Knochensubstanz entgegenwirken und Schmerzen lindern. Auch eine Bestrahlung von Knochenherden kann schmerzlindernd wirken und zur Vorbeugung von Knochenbrüchen eingesetzt werden. Bestehende Brüche müssen in der Regel durch eine Operation behandelt werden. Gebrochene Wirbelkörper können Orthopäden durch Eingabe von Knochenzement stabilisieren (Kyphoplastie, Vertebroplastie). Sind diese Maßnahmen nicht ausreichend, muss zusätzlich eine angemessene Schmerztherapie erfolgen.
In vielen Fällen ist im Verlauf der Erkrankung ein Ersatz von Blutbestandteilen, seltener auch von Immunglobulinen angebracht. Impfungen können einen gewissen Schutz vor bestimmten Infektionen (zum Beispiel Grippe, Infektion durch Pneumokokken) bieten. Ein Hyperviskositätssyndrom kann gegebenenfalls durch eine Plasmapherese behandelt werden, die überschüssige Eiweißkörper aus dem Blut "herausfiltern" kann.
Prognose: Wie sieht die Lebenserwartung mit Multiplen Myelom aus?
Eine wichtige Rolle für die Prognose spielen die vorhandenen Organschäden, wie beispielswiese eine bleibende Schädigung der Niere trotz Therapie. Darüber hinaus gibt es auch noch andere Prognosefaktoren, die in einem gewissen Rahmen eine Aussage über den wahrscheinlichen Krankheitsverlauf erlauben. Dazu gehören beispielsweise die Höhe des Albuminspiegels im Blut, die Menge des sogenannten β2-Mikroglobulins und die Art der Chromosomenveränderungen in den Tumorzellen.
Die Krankheit kann aktuell nicht geheilt werden. In vielen Fällen ist aber eine deutliche Verbesserung der Überlebenszeit und der Lebensqualitiät dank neuerer Therapieansätze möglich. Weitere Therapien und Substanzen befinden sich in der klinischen Erprobung und geben Hoffnung auf eine weitere Verbesserung.
Wichtiger Hinweis: Dieser Artikel enthält nur allgemeine Hinweise und darf nicht zur Selbstdiagnose oder –behandlung verwendet werden. Er kann einen Arztbesuch nicht ersetzen. Die Beantwortung individueller Fragen durch unsere Experten ist leider nicht möglich.