Forscherportrait: Alzheimer im Blut

Alzheimer-Forscher Christian Haass
© W & B/ Max Kratzer
Das Experimentieren mit dem eigenen Blut brachte ein erschreckendes Ergebnis: Es enthielt ein Eiweiß, das man bei Menschen mit Alzheimer erwartet hätte. Der Alzheimer-Forscher Christian Haass glaubte, selbst bald an dieser Form von Demenz zu erkranken, die das Gedächtnis, die Orientierung und zum Schluss die Selbstständigkeit zerstört. Und das bereits mit 32 Jahren. „Ich befürchtete für mich das Schlimmste“, erinnert sich der Molekularbiologe an seine Entdeckung im Jahr 1992.
Wenige Tage später beruhigte ihn jedoch das nächste Ergebnis. Das vermeintliche Alzheimer-Kennzeichen Beta-Amyloid fand sich auch im Blut seiner Kollegen. Das eigentliche Aha-Erlebnis hatte Haass einige Wochen später in der Dunkelkammer. „Ich wusste sofort: Das wird das gesamte Gebiet verändern. Und meine Zukunft als Forscher ist erst einmal gesichert.“
Schlüsselerlebnis mit Schlüsselprotein
Was er sah, ließ nur einen Schluss zu: Beta-Amyloid ist ein normales Eiweiß in gesunden Menschen und entsteht in vielen Geweben. Damit war der Weg gebahnt, es in menschlichen Zellkulturen zu erforschen. Die Basis, um herauszufinden, warum Beta-Amyloid im Gehirn Klumpen bildet – die vermutete Ursache von Alzheimer.
Haass verfiel in eine zuvor nicht gekannte Euphorie. „Das muss wie Kokain sein. Man wird abhängig.“ Er und seine Kollegen arbeiteten fieberhaft Tag und Nacht. „Das war schon ein bisschen gefährlich“, erinnert sich Haass. Er schlief kaum, kannte von Boston nicht viel mehr als den Fußweg ins Labor und zurück.
Familie oder Forschung?
Just am Tag, als das renommierte Fachblatt Nature seine Ergebnisse zur Veröffentlichung freigab, wurde seine Tochter geboren. Wenige Stunden später war er wieder im Labor. „Den Fehler würde ich nie wieder machen. Das nehme ich mir heute noch übel“, sagt Haass, der damals in einem Jahr gleich dreimal in Nature publizierte.
„Entweder mach ich etwas richtig oder gar nicht.“ So lautet Haass’ Lebensmotto, der sich selbst als „Nerd“ bezeichnet. Das englische Wort steht für oft sehr kluge Menschen, die ihre Spezialinteressen unmäßig pflegen und soziale Kontakte völlig vernachlässigen. Sonderlinge, die fast ihre gesamte Zeit vor dem Computer verbringen – oder eben im Forschungslabor.
Das große Ziel: Alzheimer stoppen
Haass ist zudem Vogel-Nerd. Bereits als Säugling krabbelte er den Tieren hinterher. Er habe wohl nur das Laufen gelernt, um ihnen schneller folgen zu können, erzählten ihm später seine Eltern. Heute fährt der mittlerweile 59-Jährige fast jeden Samstag und Sonntag an einen oberbayerischen See, um Vögel zu beobachten. „Das macht mir eine Riesenfreude. Es gibt immer wieder Neues zu entdecken.“
Seit dem Jahr 2014 ist er Sprecher am Münchner Standort des Deutschen Zentrums für Neurodegenerative Erkrankungen. „Ich bin überglücklich, das Institut hier zu haben. Es ist alles vorhanden – von der Biophysik bis zu den Patienten.“ Fast sein gesamtes Team erforscht seit einigen Jahren einen neuen Ansatz, um Alzheimer zu stoppen. Das Immunsystem soll dazu aktiviert werden, Beta-Amyloid-Klumpen im Gehirn effektiv zu bekämpfen.
Rückenwind durch Forschertrophäe
Haass erinnert sich gut an den Fachkongress, auf dem er erste Ergebnisse vorstellte. Die Koryphäe auf dem Gebiet der Alzheimer-Immunologie blaffte ihn an: „Christian, deine Forschung ist toxisch für die jungen Zuhörer hier in diesem Raum.“ Haass war sprachlos. Dann wehrte er sich. Eine hitzige Debatte entbrannte. Er hatte der Lehrmeinung widersprochen, wonach Immunreaktionen im Gehirn von Alzheimer-Patienten stets schlecht sind – und dass deshalb künftige Medikamente diese unterdrücken sollen.
Der „Brain Prize“ gab Haass Rückenwind. Im Mai 2018 erhielt er die weltweit bedeutendste Auszeichnung für einen Neurowissenschaftler. „Der Preis hätte an keinem besseren Tag kommen können. Ich war damals mit den Nerven ziemlich am Ende. Der öffentliche Unmut über die angeblich so erfolglose Amyloid-Forschung sowie übelste persönliche Anfeindungen in einer prominenten Wochenzeitung gingen mir auf den Wecker.“ Für ihn bedeutet der Preis die Bestätigung, auf der richtigen Spur zu sein.
Experten sind sich uneins
Doch bislang brachte kein Wirkstoff den erhofften Erfolg. „Die Amyloid-Hypothese ist beerdigt“, hatte der Neurowissenschaftler Dr. George Perry von der Universität von Texas in San Antonio (USA) eine fehlgeschlagene Studie im Jahr 2016 kommentiert.
Haass hält das für völligen Unsinn. „Wer so etwas behauptet, ignoriert die gesamten genetischen Erkenntnisse. Doch die Tatsachen kann man nicht einfach unter den Tisch kehren.“ Sprich: Erbgutvarianten, die die Verklumpung von Beta-Amyloid fördern, führen sehr früh im Leben zu Alzheimer. Und Varianten, die die Produktion um 20 Prozent reduzieren, schützen vor dieser Demenz-Erkrankung.
Kampf um erstes Medikament gegen Beta-Amyloid
Wird es demnächst doch das erste Medikament gegen Beta-Amyloid geben? In den USA soll demnächst ein Zulassungsverfahren beginnen. Aber die vorliegenden Testergebnisse sind widersprüchlich, die Reaktionen des Herstellers auch: Im März 2019 brach er zwei Studien mit insgesamt über 3200 Teilnehmern ab, weil die Therapie den Behandelten nichts brachte.
Haass ist empört: „Die Testpersonen erfuhren aus der Presse vom Studienabbruch. So darf man die Patienten nicht behandeln.“ Seit dem Abbruch erhalten sie auch keinen Testwirkstoff mehr. Haass: „Das ist ein Wahnsinn! Die Firmen tun so, als würden ihnen die Patienten gehören. Doch ohne Testpersonen werden wir nie ein Medikament auf den Markt bringen.“
Erneute Wendung
Im Oktober vollzog die Firma die Kehrtwende. Denn eine weitere Analyse hatte ergeben: In der höchsten Dosis verbessert das Medikament durchaus die Fähigkeit, den Alltag selbstständig zu bewältigen. Allerdings nur in einer der beiden Studien.
Haass selbst hat schon viele überraschende Wendungen erlebt. Etwa die Euphorie um die Jahrtausendwende, als die Impfung mit Beta-Amyloid in Tierversuchen erstmals Erfolg zeigte. „Damals dachten alle Experten, jetzt kommen die Medikamente zu den Patienten. Und wir Alzheimer-Forscher können nach Hause gehen.“ Doch dann kamen die vielen Fehlschläge. Bis heute gibt es nur Arzneien, die die Symptome lindern – den Gedächtnisschwund verzögern.
Fortschritt durch Fehlschläge
Haass selbst mag das Wort Fehlschlag nicht. „Wir haben bei jedem Test etwas dazugelernt.“ Erschreckend sei allerdings die Erkenntnis: Die Erkrankung wird wohl mindestens 20 Jahre vor den ersten Symptomen angelegt. Das erschwert die Behandlung enorm. Und erklärt auch, warum bisherige Studien nicht zum Erfolg führen konnten. Erst jetzt sei die Zeit reif für aussagekräftige Medikamententests.
Biomarker, die das Gehirn ins Blut freisetzt, helfen nun festzustellen, ob ein Wirkstoff im Körper einen Effekt hat. So zeigt eine aktuelle Studie mithilfe eines Blut-Biomarkers, dass eine Substanz gegen Beta-Amyloid den Tod von Nervenzellen bremst. Haass hofft, dass er bald testen lassen kann ob sich Immunzellen im Gehirn von Alzheimer-Patienten aktivieren lassen. „Wenn das funktioniert, würde für mich ein Lebenstraum in Erfüllung gehen.“
Wissenswerte Grundlagen zu Morbus Alzheimer
1. Schrecklicher Schwund von Nervenzellen
Bei Morbus Alzheimer gehen Hirnzellen zugrunde. Forscher und Firmen suchen nach Wegen, um diesen Prozess zu stoppen.
Als Erstes sterben Nervenzellen im Hippocampus ab. Dieser Bereich
ist für das Gedächtnis wichtig. Vergesslichkeit ist daher der Vorbote dieser Demenzerkrankung.
Am Ende ist das Gehirn etwa um ein Fünftel geschrumpft.
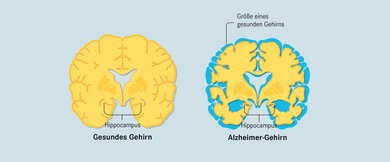
Vergleich von gesundem Gehirn und Alzheimer-Gehirn
© W&B/Astrid Zacharias
2. Stiller Anfang
Der zerstörerische Prozess beginnt viele Jahre vor der Erkrankung.
Das körpereigene Eiweiß Beta-Amyloid bildet Klumpen. Meist beginnt das im mittleren Lebensalter.
Die Verklumpung bewirkt eine zweite Veränderung: Das Eiweiß Tau bildet Fasern in den Nervenzellen.
Haben sich zu viele Tau-Fasern angesammelt, kommt es zum Tod der Nervenzellen, die betroffen sind.
Der Ausfall von Zellen führt zu einer ausgeprägten Vergesslichkeit als erstem Symptom.
Es kommt zur Demenz. Zuletzt sind viele Betroffene vollständig auf fremde Hilfe angewiesen.
3. Experimentelle Therapien
Alzheimer-Eiweiße attackieren
Ein Antikörper gegen Beta-Amyloid-Klumpen zeigte im Herbst 2019 einen kleinen positiven Effekt auf Testpersonen. In den USA prüft die Behörde die Zulassung.

Antikörper
© W&B/Astrid Zacharias
Immunzellen beeinflussen
Eine Firma in den USA testet seit Kurzem ein neues Wirkprinzip an Freiwilligen: Immunzellen im Gehirn sollen aktiviert werden, um Beta-Amyloid-Klumpen aufzulösen.

Immunzelle im Gehirn
© W&B/Astrid Zacharias



