Immun-Detektive: Wie Car-T-Zellen Krebs aufspüren
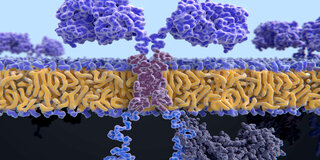
Durch die CAR-T-Therapie erkennen T-Zellen ihr Ziel besser und töten die Krebszellen ab
© mauritius images / Science Sourc
Gegen Krebs ist das menschliche Immunsystem eigentlich gut gerüstet. Eigentlich. Mehrere Akteure der Körperabwehr, darunter auch T-Zellen, erkennen die entarteten Zellen und töten sie ab. Doch Krebszellen nutzen diverse molekulare Tricks, mit denen sie diesem Angriff entgehen können.
Die sogenannte CAR-T-Therapie versucht, die T-Zellen in diesem Kampf zu stärken. Dazu versehen Forscherinnen und Forscher sie mit Erkennungsmolekülen (Rezeptoren), die sie mit Stimulatoren kombinieren. Auf diese Weise erkennen T-Zellen ihr Ziel besser und töten die Krebszellen ab.
Weil die Rezeptoren verschiedene unterschiedliche Teile in sich vereinen, nennt man sie „chimäre AntigenRezeptoren“ (CAR), die damit ausgestatteten Zellen „CAR-T-Zellen“. 2018 hat die Europäische Union die beiden ersten CAR-T-Therapien zugelassen. Sie wirken gegen bestimmte Formen von Leukämie und Lymphomen. Seither kamen weitere Präparate hinzu.
Herstellung von CAR-T-Zellen
Zur Produktion von CAR-T-Zellen werden der Patientin oder dem Patienten sogenannte T-Zellen des Immunsystems entnommen. Diese werden in spezialisierten Laboren gentechnisch mit einem chimären Antigen-Rezeptor (CAR) bestückt, der die T-Zelle gleichsam scharf stellt.
Warum wird aktuell darüber geredet?
Inzwischen wurden einige zusätzliche CAR-T-Präparate zugelassen, auch für das Multiple Myelom, einen Knochenmarkkrebs. Weitere stehen kurz davor. Wie gut sie langfristig wirken, lässt sich bisher nur für die beiden 2018 zugelassenen und zuvor in Studien untersuchten beurteilen.
Von den Patientinnen und Patienten, die wegen eines Lymphoms behandelt wurden, lebten nach fünf Jahren noch 42 Prozent. Bei den von Leukämie Betroffenen lag die Überlebensrate nach vier Jahren bei 36 Prozent. Auffällig: Todesfälle traten vor allem im ersten Jahr nach der Therapie auf.
Bei jenen, bei denen die Therapie das Fortschreiten der Krankheit gestoppt hatte, war dies meist auch nach Jahren noch der Fall. Wegen der oft erheblichen Nebenwirkungen auf Immunsystem, Gehirn und Blutzellen müssen laut einer Erhebung allerdings 14 Prozent der Behandelten intensivmedizinisch versorgt werden – wobei sich diese Rate dank eines Antikörper-Medikaments und Kortison schon deutlich gebessert hat.
Besondere Aufmerksamkeit erlangten spektakuläre Einzelfälle. Zwei Männer, die in einer der ersten CAR-T-Studien gegen eine Leukämie behandelt wurden, sind noch nach zehn Jahren krankheitsfrei. Und die im Alter von fünf Jahren als erstes Kind so therapierte Emily Whitehead feierte im Mai ihren 17. Geburtstag.
Worauf dürfen Kranke künftig hoffen?
Noch birgt das CAR-T-Konzept Wissenslücken. Erste Vergleichsstudien belegen jedoch, dass CAR-T-Zellen in ihren Einsatzgebieten deutlich besser wirken als bisherige Standardtherapien. Bisher dürfen sie jedoch erst eingesetzt werden, wenn andere Behandlungen fehlgeschlagen sind.
Bedauerlich ist, dass die CAR-T-Therapie zwar bei verschiedenen Formen von Krebs im Blut, im Lymphsystem und im Knochenmark funktioniert – bei Organtumoren aber noch vor Hürden steht. Auch hierzu gibt es indes erste hoffnungsvolle Versuche: etwa bei Lungen- oder Darmkrebs.
„Die Herausforderung besteht darin, krebsspezifische Angriffsziele zu finden“, sagt Professorin Marion Subklewe, CAR-T Expertin an der LMU-Uniklinik München. Denn sonst würden auch gesunde Zellen zerstört. Ein großes Problem sind die Kosten der Therapie. Die beiden zuerst zugelassenen Präparate etwa kosten 275 000 beziehungsweise 282 000 Euro für eine im Idealfall einmalige Behandlung. Allerdings gibt Marion Subklewe zu bedenken: Die Gesamtkosten für andere Behandlungen, die langfristig eingesetzt werden müssen, sind auch nicht immer geringer.
Quellen:
- EMA: First cell-based gene therapy to treat adult patients with multiple myeloma. https://www.ema.europa.eu/... (Abgerufen am 02.05.2022)
- Leidford H: LAST-RESORT CANCER THERAPY HOLDS BACK DISEASE FOR A DECADE, Two of the first people treated with CAR-T-cell cancer therapies are still in remission 12 years on. In: Nature 10.02.2022, 602: 196
- King A: The less-personal touch, CAR-T immunotherapy is a specialist and complex treatment for cancer. Now, researchers are looking to provide an off-the-shelf version to make the therapy available to more people. In: Nature 24.09.2020, 585: 84-86
- Willen C: Innovationen der Immuntherapien: CART- Zellen – allogen, biphasisch oder im Tandem. In: Deutsches Ärzteblatt 04.02.2022, 119: 180-182
- Zhang C: Phase I Escalating-Dose Trial of CAR-T Therapy Targeting CEA+ Metastatic Colorectal Cancers. In: Molecular Therapy 05.05.2017, 25: 1248-1257
- Biontech: BioNTech Presents Positive Preliminary Phase 1/2 Data for First-in-Class CAR-T Program BNT211 at AACR. https://investors.biontech.de/... (Abgerufen am 03.05.2022)
- Changsong Q: Claudin18.2-specific CAR T cells in gastrointestinal cancers: phase 1 trial interim results. In: Nature medicine 09.05.2022, 623: 1-10
- Paul-Ehrlich-Institut: Europäische Kommission erteilt Zulassung für zwei CAR-T-Zelltherapeutika. https://www.pei.de/... (Abgerufen am 22.04.2022)
- Elise A. Chong, M.D. Marco Ruella, M.D. Stephen J. Schuster, M.D.: Five-Year Outcomes for Refractory B-Cell Lymphomas with CAR T-Cell Therapy. In: New England Journal of Medicine 18.02.2021, 348: 673-674
- Jae H. Park et al.: Long-Term Follow-up of CD19 CAR Therapy in Acute Lymphoblastic Leukemia. In: New England Journal of Medicine 01.02.2018, 378: 449-459
- J. Joseph Melenhorst et al.: Decade-long leukaemia remissions with persistence of CD4+ CAR T cells. In: Nature 17.02.2022, 602: 505
- Locke FL et al.: Axicabtagene Ciloleucel as Second-Line Therapy for Large B-Cell Lymphoma. In: New England Journal of Medicine 17.02.2022, 386: 640-654
- Maude SL: Tisagenlecleucel in Children and Young Adults with B-Cell Lymphoblastic Leukemia. In: New England Journal of Medicine 01.02.2018, 378: 439-448
- Schuster SJ et al.: Long-term clinical outcomes of tisagenlecleucel in patients with relapsed or refractory aggressive B-cell lymphomas (JULIET): a multicentre, open-label, single-arm, phase 2 study. In: Lancet Oncology 01.10.2021, 22: 1403-1415
- Bishop MR: Second-Line Tisagenlecleucel or Standard Care in Aggressive B-Cell Lymphoma. In: New England Journal of Medicine 17.02.2022, 386: 629-639
- Universimed: Jede Behandlung ein Unikat: Zelltherapien aus der Perspektive der Transfusionsmedizin. https://www.universimed.com/... (Abgerufen am 27.04.2022)
- Winnat C: 26 CAR-T-Zentren und bisher weniger Patienten als erwartet, DGHO-Bilanz. Deutsche Ärztezeitung: https://www.aerztezeitung.de/... (Abgerufen am 20.05.2022)
- Osterloh F: In der Versorgung angekommen, CAR-T-Zell-Therapie. In: Deutsches Ärzteblatt 04.02.2022, 119: 176-178
- Sonnet M: Optimierung der CAR-T-Zell-Therapie, Bispezifische CAR-T-Zellen auf dem Prüfstand. In: InFo Hämatologie + Onkologie 01.03.2022, 25: 50