Was ist eine rheumatoide Arthritis?
Rheumatoide Arthrits: Was ist das?
Rheumatische Erkrankungen, im Volksmund kurz "Rheuma" genannt, umfassen über 100 verschiedene Krankheitsbilder, die durch Abnutzungen (Arthrose), Entzündungen oder Stoffwechselstörungen hervorgerufen werden und die vorwiegend das Bewegungssystem betreffen. Die rheumatoide Arthritis ist die häufigste rheumatisch-entzündliche – also durch das Immunsystem verursachte – Gelenkerkrankung. Sie hat nichts mit mechanischer Abnutzung wie bei der Arthrose zu tun.
Bei rheumatisch-entzündlichen Erkrankungen schleicht sich im Verlauf von Jahren unbemerkt ein Fehler des Immunsystems ein. Das Immunsystem besteht vor allem aus den weißen Blutkörperchen (Leukozyten) und dient der Abwehr von Viren, Bakterien, Giften und Krebszellen. Durch diesen Fehler können Teile des Immunsystems nicht mehr richtig zwischen körpereigen und körperfremd unterscheiden. Körpereigenes Gewebe, das das Immunsystem eigentlich in Ruhe lassen soll, wird angegriffen: Die Entzündung befällt bei der rheumatoiden Arthritis vorwiegend die Innenhaut (Membrana synovialis) von Gelenken, Sehnenscheiden und Schleimbeuteln. Die Gelenkinnenhaut produziert die Gelenkflüssigkeit. Diese dient zur Ernährung des Gelenkknorpels und gleichzeitig als Schmiersubstanz, um die Reibung an den Gelenkflächen zu reduzieren.
Eine rheumatoide Arthritis kann plötzlich, aber auch schleichend auftreten. Erste Anzeichen sind Schwellungen, Überwärmung sowie morgendliche Steifheit der Gelenke. Die Beschwerden sind meist symmetrisch und treten häufig zunächst an den Grund- und Mittelgelenken der Finger oder Zehen sowie den Handgelenken auf. Es können aber auch andere Gelenke wie Knie, Schulter, Hüft- oder Fußgelenke und auch die obere Halswirbelsäule betroffen sein.
Typisch ist ein Verlauf in Schüben, die über mehrere Wochen anhalten. Es kann zu Gelenkverformungen bis zur kompletten Gelenkzerstörung kommen. Seltener sind andere Organe, wie Tränen- oder Speicheldrüsen, Lunge, Herz, Blutgefäße und Augen beteiligt.
In Deutschland ist circa ein Prozent der Bevölkerung von der rheumatoiden Arthritis betroffen, Frauen etwa dreimal so häufig wie Männer. Die rheumatoide Arthritis kann in jedem Lebensalter auftreten, sogar im Kindesalter (polyartikuläre juvenile idiopathische Arthritis). Mit zunehmendem Alter nimmt bei beiden Geschlechtern auch die Erkrankungshäufigkeit zu. Die Krankheit beginnt meist im vierten bis fünften Lebensjahrzehnt.
Prognose der rheumatoiden Arthritis
Die Prognose der rheumatoiden Arthritis ist abhängig von der Krankheitsaktivität bei Beginn und im Verlauf sowie davon, wann die medikamentöse Therapie einsetzt. Der Nachweis von Rheumafaktoren oder Anti-citrullinierte-Peptid/Protein-Antikörpern (ACPA) deutet eher auf einen aggressiveren Krankheitsverlauf hin.
Das Ziel der Behandlung ist eine möglichst vollständige Rückbildung der Krankheitsaktivität (Remission) und die Verhinderung der Gelenkzerstörung und von Funktionsverlust. Dies gelingt mit den heutigen Therapiemöglichkeiten bei einem Großteil der Patienten, die konsequent behandelt werden. Eine kontinuierlicher Therapie muss durch eine ständige Überwachung von Wirkung und Nebenwirkungen durch Hausarzt und Rheumatologen begleitet werden.
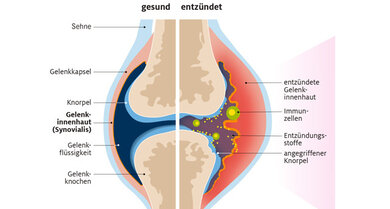
Rheumatoide Arthritis: Das passiert im entzündeten Gelenk
© W&B/W&B/Dr. Ulrike Möhle
Ursachen: Was passiert im Gelenk?
Die Ursachen der rheumatoiden Arthritis sind noch nicht abschließend geklärt. Das Immunsystem spielt bei der Krankheitsentstehung die entscheidende Rolle.
Das Immunsystem besteht vor allem aus weißen Blutkörperchen und ist im gesunden Körper in der Lage, körpereigene von körperfremden Substanzen zu unterscheiden. Bei einer rheumatisch-entzündlichen Erkrankung – auch Autoimmunerkrankung – schleicht sich im Verlauf von Jahren unbemerkt ein Fehler im Immunsystem ein, sodass der Körper bestimmte eigene Substanzen als fremd ansieht. Die Folge ist eine Reaktion des Immunsystems in Form einer Entzündung.
Bei der rheumatoiden Arthritis wandern fehlgesteuerte Immunzellen in die Gelenke und produzieren dort verschiedene entzündungsfördernde Stoffe wie zum Beispiel Gewebshormone, sogenannte Zytokine. Diese sind für die Zellkommunikation zuständig. Normalerweise befinden sich die Zytokine im Gleichgewicht mit Gegenspielern (Antagonisten). Dies verhindert überschießende Immunreaktionen. Durch die vermehrte Produktion von Zytokinen wird dieses fein abgestimmte Gleichgewicht gestört.
Zytokine, die bei der rheumatoiden Arthritis eine wichtige Rolle spielen, sind der Tumornekrosefaktor-Alpha (TNF-alpha) und das Interleukin-6 (IL-6). Daneben sind aber auch noch andere solche Gewebshormone am Fortschreiten der Erkrankung beteiligt.
Der Entzündungsprozess führt dazu, dass die Gelenkinnenhaut stark wuchert. Aus den Blutgefäßen tritt vermehrt Flüssigkeit aus, wodurch es zu einem Gelenkerguss kommen kann. Nach einiger Zeit zerstört die wuchernde Gelenkinnenhaut Knorpel, Knochen und Bänder des Gelenks. Weiße Blutkörperchen lösen abgestorbene Gewebeteilchen auf und setzen dabei noch mehr Zytokine frei, wodurch der Knorpel weiter geschädigt wird.
Als Auslöser für die immunologische Fehlsteuerung werden verschiedene Faktoren diskutiert: Eine wichtige Rolle scheint das Rauchen zu spielen. Möglicherweise sind auch Infektionserreger (Viren und Bakterien) von Bedeutung. Erbliche Einflüsse sind ebenfalls beteiligt. Wahrscheinlich ist, dass mehrere Faktoren über mehrere Jahre zusammen kommen müssen, um eine rheumatoide Arthritis auszulösen. Der die Krankheit bedingende Fehler des Immunsystems ist zu komplex, als dass er in kurzer Zeit von einer einzelnen Ursache ausgelöst werden könnte.
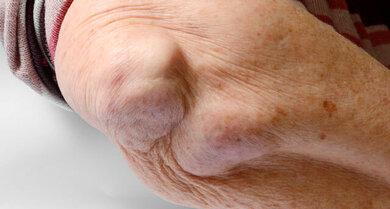
Bei manchen Patienten treten sogenannte Rheumaknoten auf
© Science Photo Library/-
Symptome
Zu Beginn der Erkrankung kann es zu ganz unspezifischen Symptomen kommen, zum Beispiel zu:
- Müdigkeit
- Erschöpfungszuständen
- Appetitlosigkeit
- Gewichtsabnahme
- Temperaturen bis 38° oder sogar Fieber
Bei manchen Patienten setzt diese Phase schlagartig ein, bei anderen eher schleichend. In dieser frühen Erkrankungsphase ist es besonders schwierig, die Diagnose zu stellen.
Symptome am Bewegungsapparat
Gleichzeitig entwickeln die meisten Patienten typische Symptome am Bewegungssystem, deren Verlauf und Intensität ganz unterschiedlich sein kann. Dazu gehören:
- Morgensteifigkeit: Vor allem morgens haben die Betroffenen steife und schmerzende Gelenke. Meist sind die Finger betroffen. Die Beschwerden können mehrere Stunden andauern und bessern sich dann allmählich.
- Gelenkentzündung: Die Gelenke schwellen an und schmerzen, sind überwärmt, aber nur ganz selten gerötet. Schmerzen durch die Gelenkentzündung treten häufig in Ruhe auf, oft sind sie in der zweiten Nachthälfte am stärksten. Druck auf das Gelenk und maximale Beugung oder Streckung verstärken die Schmerzen. Meist sind auf beiden Körperseiten die Fingergrund- und –mittelgelenke, die Handgelenke sowie die Zehengrundgelenke betroffen, später geht die Entzündung auch auf andere große und kleine Gelenke über (Polyarthritis). Die Gelenke verformen sich, die Beweglichkeit nimmt ab.
- Sehnenscheidenentzündung (Tendovaginitis): Schwellung und Schmerzen meist im Hand- und Sprunggelenksbereich. Durch Schädigung benachbarter Nerven können Nervenschmerzen oder Missempfindungen entstehen (zum Beispiel ein Karpaltunnel-Syndrom mit Taubheit von Daumen, Zeige- und Mittelfinger)
- abnehmende Greifkraft der Hände: Diese fällt Betroffenen oft früh auf und führt zu zunehmenden Schwierigkeiten bei Alltagstätigkeiten, wie zum Beispiel dem Aufschrauben von Marmeladengläsern
- Rheumaknoten: An den Streckseiten der Gelenke, vor allem an den Ellenbogen und Händen, aber auch an der Achillessehne und der Unterschenkelvorderseite, entwickeln sich bei etwa 20 Prozent der Patienten gutartige, derbe und teilweise verschiebliche Knoten unter der Haut oder direkt an den Sehnen
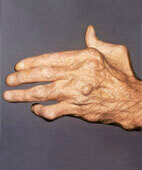
Bei einer rheumatoiden Arthritis können sich Fehlstellungen der Gelenke entwickeln
© Science Photo Library/BiohotoAssociates
Fehlstellungen der Gelenke
Im weiteren Krankheitsverlauf entwickeln sich typische Fehlstellungen der Gelenke:
- Abweichung der Hand nach außen in Richtung des kleinen Finger
- Fixierte Beugestellung im Fingermittelgelenk und Überstreckung im Fingerendgelenk (Knopflochdeformität)
- Fixierte Beugestellung des letzten Fingergliedes bei gleichzeitiger Überstreckung im Fingermittelgelenk (Schwanenhalsdeformität)
- Fixierte Beugestellung im Daumengrundgelenk und Überstreckung des Daumenendgelenkes
Beteiligung anderer Organsysteme
In seltenen Fällen können auch andere Organsysteme wie Blutgefäße, Herz, Lunge, Speichel- oder Tränendrüsen und Augen von der rheumatoiden Arthritis betroffen sein:
- Chronische Entzündung und Trockenheit von Mund und Augen (Sicca-Syndrom)
- Entzündung der Blutgefäße (Vaskulitis)
- Herzbeutelentzündung
- Entzündung mit Bindegewebsvermehrung der Lunge (Lungenfibrose) und Rippenfellentzündung (Pleuritis)
- Entzündungen von Hornhäuten und Bindehaut der Augen (Skleritis, Episkleritis)
Erhöhtes Risiko für andere Krankheiten
Die Rheumatoide Arthritis erhöht das Risiko für bestimmte, weitere Erkrankungen. Komorbidität nennen Mediziner dieses gleichzeitige Auftreten unterschiedlicher Krankheiten. Diese zusätzlichen Leiden können die Patienten in ihrem Alltag belasten und unter Umständen sogar ihre Lebenserwartung mindern. Dazu gehören:
- Arteriosklerose ("Gefäßverkalkung"). Die Gefahr steigt, einen Herzinfarkt oder Schlaganfall zu erleiden
- Osteoporose (Knochenschwund)
- chronisch generalisierte Schmerzsyndrome
- Infektionen
- Depression und Angststörungen
- Lymphome (bösartige Erkrankungen bestimmter Abwehrzellen)
Bestimmte Antikörper im Blut können auf eine rheumatoide Arthritis hinweisen
© Panthermedia/Josef Müllek
Diagnose
Je früher die rheumatoide Arthritis erkannt und behandelt wird, desto besser lässt sich die Gelenkzerstörung hemmen. Gerade in der Frühphase der Erkrankung, in der die Symptome noch sehr unspezifisch sind (siehe Kapitel Symptome), ist die Diagnosestellung allerdings oftmals schwierig.
Die Krankengeschichte des Patienten kann hier wegweisend sein. Bei der Untersuchung zeigen sich dem Arzt eventuell schon die typischen Gelenkveränderungen. Bluttests und bildgebende Verfahren, wie Röntgenuntersuchungen tragen dann dazu bei, den Verdacht auf eine rheumatoide Arthritis zu erhärten. Bei einer frühen Rheumatoiden Arthritis können die Röntgenveränderungen allerdings fehlen. Denn Röntgenaufnahmen zeigen vor allem, ob es bereits zu einem Schaden gekommen ist. Andere Untersuchungsmethoden wie Ultraschalluntersuchungen (Sonografie), Magnetresonanztomografie und Szintigrafie liefern in solchen fühen Stadien oft Hinweise auf die aktive Entzündung.
Viele Rheumatologische Praxen und Zentren bieten mittlerweile Sprechstunden für die Frühdiagnostik der Rheumatoiden Arthritis an. Überwiesen durch den Hausarzt, ist es dort möglich, einen kurzfristigen Termin bei einem Rheumatologen (Spezialist für rheumatische Erkrankungen) zur Untersuchung zu bekommen. So kann bei Bestätigung der Diagnose eine möglichst rasche Therapie erfolgen.
Klassifikations-Kriterien
Im Gegensatz zu vielen anderen Erkrankungen kann man die rheumatoide Arthritis nicht anhand eines einzigen Tests klar diagnostizieren. Die Diagnosestellung erfolgt, indem der Experte ein Erkrankungsmuster erkennt, also ein Mosaik aus mehreren Bausteinen und andere Ursachen dafür ausschließt. Um dem Rechnung zu tragen haben rheumatologische Fachgesellschaften Diagnose- oder Klassifikationskriterien erstellt. Die Klassifikationskriterien des American College of Rheumatology (ACR) und der European League Against Rheumatism (EULAR) aus dem Jahr 2010 können bei der Diagnosefindung als Orientierung dienen. Berücksichtigt und nach einem Punkteschema gewertet werden dabei:
- die Anzahl und Art der beteiligten Gelenke
- die Dauer der Gelenkentzündung (kürzer oder länger als sechs Wochen)
- Ergebnisse von Blutuntersuchungen (Rheumafaktor, Autoantikörper gegen citrullinierte Peptide, Entzündungsparameter wie CRP, BSG – mehr dazu weiter unten im Text)
Eine besonders hohe Bedeutung für diese Kriterien hat die Erosivität, also die Tatsache, dass die Gelenkentzündung zu Knochenlöchern oder -schäden geführt hat. Wichtig zu wissen: Klassifikationskritieren sind für die individuelle Diagnosestellung hilfreich, aber nicht entscheidend.
Wie aktiv die Krankheit im Moment ist und wie gut die begonnene Therapie anschlägt, lässt sich mit Hilfe eines anderen Wertes einschätzen – dem sogenannten "Disease Activity Score" (DAS, Krankheits-Aktivitäts-Score) der EULAR. Der Arzt ermittelt dazu die Zahl der geschwollenen oder druckschmerzhaften Gelenke, berücksichtigt den Blutwert BSG und fragt nach dem subjektiven Empfinden des Patienten. Es ergibt sich ein Punktwert, der auf eine fehlende, niedrige, mittlere oder hohe momentane Krankheitsaktivität schließen lässt.
Körperliche Untersuchung
Der Arzt untersucht meist alle Gelenke (nicht nur die betroffenen) auf Schwellung, Druckempfindlichkeit, Funktionsbeeinträchtigung und sucht nach Rheumaknoten sowie nach Hinweisen auf eine Organbeteiligung und Begleiterkrankungen.
Blutuntersuchung
Anhand der im Blut messbaren erhöhten Entzündungswerte (Blutsenkungsgeschwindigkeit (BSG), C-reaktives Protein (CRP)) lässt sich abschätzen, wie aktiv die Krankheit ist. Allerdings sind diese Werte zu Beginn der Erkrankung nicht selten normal und andererseits auch bei anderen chronischen und akuten Entzündungen oder Infektionen erhöht.
Bei ungefähr 85 Prozent der Patienten finden sich im Blut Rheumafaktoren und/oder Anti-citrullinierte-Protein/Peptid-Antikörper (ACPA). Dabei handelt es sich um Autoantikörper, also Antikörper, die gegen bestimmte körpereigene Substanzen gerichtet sind. Rheumafaktoren gelten als relativ unspezifisch, weil sie mit zunehmendem Alter auch in der gesunden Normalbevölkerung vorkommen. Dagegen sind die ACPAs hochspezifisch. Bei einem eindeutigen ACPA-Nachweis liegt mit hoher Wahrscheinlichkeit bereits eine rheumatoide Arthritis vor oder sie wird sich in den nächsten Jahren entwickeln. Die früher übliche alleinige Bestimmung von Rheumafaktoren (ohne ACPA-Bestimmung) ist zur Abklärung bei Verdacht auf rheumatoide Arthritis folglich nicht sinnvoll. Anders herum betrachtet ist eine rheumatoide Arthritis bei fehlendem Nachweis von Rheumafaktoren oder ACPA keinesfalls ausgeschlossen.
Bei bereits länger dauernder, unbehandelter rheumatoider Arthritis kann auch das Blutbild im Sinne einer Blutarmut, bedingt durch die Entzündung, verändert sein (Entzündungsanämie).

Ein Röntgenbild der Hände kann Gelenkveränderungen nachweisen
© PhotoDisc/ RYF
Bildgebende Untersuchungen
Üblicherweise werden zum Nachweis der für die Erkrankung typischen Gelenkveränderungen Röntgenbilder der betroffenen Gelenke und Hände sowie Füße angefertigt. Das Röntgenbild kann zunächst unauffällig sein. Typische Veränderungen sind Knochendefekte am äußeren Rand der Gelenkflächen, gelenknaher Kalksalzmangel im Knochen (Osteoporose) und Gelenkfehlstellungen.
Mit Ultraschall können entzündliche Veränderungen der Gelenke, Sehenscheiden und Schleimbeutel gut beurteilt werden. Auch die diagnosebestimmenden Knochendefekte entdeckt der Arzt mittels der Sonografie meist früher als im Röntgenbild. Andere bildgebende Verfahren, wie die Magnetresonanztomografie und die Szintigrafie können bei speziellen Fragstellungen ebenfalls hilfreich sein.

Bei der Behandlung der rheumatoiden Arthritis sind neben dem Arzt oft weitere Berufsfelder gefragt
© iStock/claudiobaba
Therapie der rheumatoiden Arthritis
Die rheumatoide Arthritis sollte ganzheitlich behandelt werden. Die bestmögliche Therapie ist daher nur durch ein Zusammenspiel von Haus- und Fachärzten (Rheumatologen, Orthopäden und Chirurgen), Physio- und Ergotherapeuten, Psychologen und Sozialarbeitern möglich. Der internistische Rheumatologe sollte die Therapie führen und der Behandlungsplan sollte eine gemeinsame und individuell an den Bedürfnissen des Betroffenen ausgerichtete Entscheidung von Patient und Arzt sein.
Ziel der Therapie ist die bestmögliche Hemmung entzündlicher Prozesse, die Schmerzlinderung und der Erhalt von Funktion und Kraft der Gelenke. Dies wird vor allem durch die frühzeitige und kontinuierlich angepasste medikamentöse Therapie mit klar definierten Zielen erreicht. Insgesamt stützt sich die Behandlung auf mehrere Säulen:
• Medikamente
• Injektionstechniken und operative Verfahren
• Physikalische Therapie
• Psychologische Therapie
• Ernährung
• Patientenschulung
Medikamentöse Therapie
Die medikamentöse Behandlung besteht in der Regel in der Kombination verschiedener Therapieprinzipien mit dem Ziel möglichst rasch Schmerzen, Entzündungs- und Schädigungsprozesse zu unterdrücken. In erster Linie werden hierzu die entzündungshemmenden Glukokortikoide und den Krankheitsverlauf beeinflussende Basistherapeutika eingesetzt und ergänzend bei Bedarf sogenannte nichtsteroidale Antirheumatika, andere Schmerzmittel und lokale Injektionen, also Spritzen mit Glukokortikoiden in die Gelenke. Das Spritzen von radioaktiven Substanzen in die Gelenke (Radiosynoviorthese) ist nur speziellen Situationen vorbehalten und wird immer seltener durchgeführt. Auch operative Verfahren wie die Synoviektomie kommen in manchen Fällen zum Einsatz.
Basistherapie, Biologika, Biosimilars und "small molecules"
Basistherapie allgemein:
Die Basistherapie verfolgt das Ziel, die Entzündung, die Gelenkzerstörung und das Voranschreiten der Krankheit zu bremsen. Aus diesem Grunde sollte möglichst frühzeitig damit begonnen werden. Ein Erfolg ist oft erst nach einigen Monaten zu verzeichnen, da sich die volle Wirkung der meisten Medikamente erst nach vier bis 16 Wochen entfaltet. Umso wichtiger ist die konsequente Einnahme der Basistherapie. Denn sie lässt sich nicht nach der kurzfristigen Wirkung dosieren. Dabei ist sie entscheidend für den Krankheitsverlauf und die Verhinderung von chronischem Schaden.
Basistherapeutika unterdrücken verschiedene Entzündungsmechanismen und können die Krankheit so eindämmen. Wegen der möglicherweise kritischen Nebenwirkungen sind regelmäßige Kontrollen der Blutwerte nötig. Dies ist umso wichtiger, da die Therapie meistens über mehrere Jahre erfolgen muss.
Konventionelle, synthetische Basistherapeutika:
Methotrexat ist das am häufigsten eingesetzte Basistherapeutikum und das Medikament mit den längsten Erfahrungen bezüglich der Sicherheit als Langzeittherapie. Alternativ oder in Kombination kann auch Leflunomid verwendet werden.
In leichteren Fällen kann auch Sulfasalazin oder das Malariamittel Chloroquin helfen: Diese beiden Substanzen entfalten aber fast nur in Kombination mit anderen Basistherapeutika eine ausreichende Wirkung. Weitere Basistherapeutika, die aber kaum noch angewandt werden, sind Ciclosporin, Azathioprin und Goldsalze. Häufig müssen verschiedene Basismedikamente miteinander kombiniert werden, um die gewünschte Wirkung zu erzielen.
Die häufigsten Nebenwirkungen unter einer Therapie mit Basistherapeutika sind Veränderungen des Blutbildes, Störungen der Nieren- und Leberfunktion, Magen-Darm-Beschwerden, Müdigkeit und Kopfschmerzen. Nach Absetzen der Medikamente verschwinden diese Beschwerden meist, bleibende Schäden sind die absolute Ausnahme.
Biologika, Biosimilars und "small molecules":
Die sogenannten Biologika sind gentechnisch hergestellte Basistherapeutika. Durch Nachahmung körpereigener Eiweißbestandteile des Immunsystems gelingt mit ihnen eine gezieltere Hemmung von Entzündungsvorgängen, die für die rheumatoide Arthritis spezifisch und entscheidend sind. Manche Biologika sind Hemmstoffe von Entzündungsbotenstoffen (Zytokine, wie zum Beispiel TNF-alpha) oder deren Rezeptoren. Andere Biologika binden und hemmen verschiedene Immunzellen (B-Zellen, T-Zellen).
Eine Auflistung der aktuell für die rheumatoide Arthritis zugelassenen Biologika und deren Wirkmechanismus ergibt die folgende Tabelle:
|
Biologika |
Wirkmechanismus und Besonderheiten |
|---|---|
|
Infliximab, Etanercept, Adalimumab, Golimumab, Certolizumab |
Hemmung des Botenstoffes TNF-alpha |
|
Tocilizumab, Sarilumab |
Hemmung des Interleukin-6-Rezeptors |
|
Rituximab |
Hemmung der B-Zellen |
|
Abatacept |
Hemmung der T-Zell-Kostimulation |
|
Anakinra |
Hemmung des Interleukin-1-Rezeptors, Anakinra wird bei der rheumtoiden Arthritis nur noch selten verwendet |
Biologika werden vor allem dann eingesetzt, wenn die Krankheit mit konventionellen, synthetischen Basistherapeutika wie Methotrexat nicht ausreichend unterdrückt werden kann. Eine Therapie mit Biologika ist relativ teuer. Mittlerweile sind für manche Substanzen günstigere Nachahmerpräparate auf dem Markt, die sogenannten Biosimilars. Die Deutsche Gesellschaft für Rheumatologie (DGRh) hat sich bereits dahingehend geäußert, dass man in den meisten Fällen bedenkenlos von einem Orginal-Biologikum auf ein Biosimilar wechseln oder auch mit einem Biosimilar die Biologika-Therapie beginnen kann.
Meist werden Biologika mit Methotrexat kombiniert. Da es sich um relativ große Eiweißmoleküle handelt, müssen Biologika in die Vene oder in das Unterhautfettgewebe gespritzt werden.
Seit 2017 sind in Deutschland zwei Substanzen einer neuen Generation von Basistherapeutika erhältlich, die sogenannten "small molecules". Sie greifen ähnlich gezielt wie die Biologika in das Immunsystem ein, sind aber so kleine Moleküle, dass sie als Tabletten eingenommen werden können. Diese Medikamente heißen Tofacitinib und Baricitinib und hemmen Januskinasen (JAK) – bestimmte Eiweißmoleküle zur Signalübertragung in der (Entzündungs-)Zelle.
Wie bei jeder Basistherapie müssen auch bei den Biologika und den "small molecules" gemeinsam mit dem Arzt alle möglichen Vorteile und Nachteile sorgfältig abgewogen werden. Langfristige unerwünschte Wirkungen sind mittlerweile durch Medikamentenregister für die meisten Substanzen relativ gut untersucht.
Das Infektionsrisiko wird durch Basistherapeutika je nach Substanz nicht (zum Beispiel bei Methotrexat) oder nur mäßig (zum Beispiel bei Biologika) erhöht. Zum Vergleich – die Therapie mit Kortikosteroiden beeinflusst das Infektionsrisiko meist stärker: zum Beispiel erhöhen zehn Milligramm Prednisolon, eine durchaus übliche Kortikosteroiddosis, das Infektionsrisiko mehr als eine Biologikatherapie. Entgegen einer früheren Befürchtung erhöhen Basistherapeutika nach aktuellem Kenntnisstand nicht das Risiko für bösartige Erkrankung. Für einzelne Substanzen existieren lediglich Hinweise für eine leichte Erhöhung des Hautkrebsrisikos. Patienten mit Autoimmunerkrankungen wie der rheumatoiden Arthritis sollten sich aber sowieso regelmäßig beim Hautarzt zur Krebsvorsorge vorstellen, damit Hautkrebs rechtzeitig entdeckt werden kann.
Aufgrund der mittlerweile großen Auswahl von Basistherapeutika gelingt es in fast allen Fällen für die Patienten ein Medikament auszusuchen, das den gewünschten Effekt erzielt und keine Nebenwirkungen hat, die sich so stark auf den Patienten auswirken, dass der positive Nutzen nicht überwiegen würde.
Kortikosteroide
Kortikosteroide (auch Glukokortikoide oder kortisonartige Substanzen) wirken entzündungshemmend und unterdrücken die überschießende Reaktion des Immunsystems. Sie können auf diese Weise dazu beitragen, die durch die Erkrankung hervorgerufenen Schäden zu minimieren. Eingesetzt werden diese Stoffe zum Beispiel um die Zeit, bis eine Basistherapie zu wirken beginnt, zu überbrücken, aber auch als längerfristige Therapieoption. Da ein Knochenschwund (Osteoporose) eine Nebenwirkung bei regelmäßiger Einnahme dieser Medikamente ist, sollte dem gegebenenfalls durch eine ausreichende Zufuhr von Kalzium und Vitamin D oder bestimmten Medikamenten – beispielsweise Bisphosphonaten – vorgebeugt werden. Über mögliche Nebenwirkungen dieser Arzneien informiert der Arzt. Bei richtigem Einsatz sind Kortikosteroide ein Segen für die Patienten, bei falschem Einsatz in zu hoher Dosis und/oder über zu lange Zeit bergen sie jedoch Risiken. Nichts hemmt so schnell die Entzündung wie Kortikosteroide; dadurch sind sie für die Behandlung der rheumatoiden Arthritis bis auf wenige Ausnahmen zumindest für die Anfangsphase weiterhin unverzichtbar. Dagegen ist eine Kortikosteroiddauertherapie mit einer Dosis, die mehr als fünf Milligramm Prednisolon entspricht, möglichst zu vermeiden, da sie zu Arteriosklerose, Osteoporose und Infektionen führen kann.
Schmerztherapie
Nichtsteroidale Antirheumatika:
Um die Schmerzen und die Entzündung zu hemmen, werden hauptsächlich nichtsteroidale Antirheumatika (NSAR), wie zum Beispiel Diclofenac und Ibuprofen eingesetzt. Sie haben als gemeinsames Wirkprinzip die Hemmung des Enzyms Cyclooxygenase, welches unter anderem zur Produktion von Entzündungsstoffen, den Prostaglandinen, notwendig ist. Der entzündungshemmende Effekt ist aber bei der rheumatoiden Arthritis meistens nicht mit den Kortikosteroiden vergleichbar.
Unser Video zeigt Ihnen, wie diese Schmerzmittel wirken:
Cyclooxygenase-Hemmer können bei Bedarf oder seltener über längere Phasen angewandt werden. Dabei steigt jedoch das Risiko für Magen-Darm-Geschwüre, insbesondere wenn zusätzlich Kortikosteroide eingenommen werden. Denn die von der Cyclooxygenase hergestellten Prostaglandine spielen auch eine wichtige Funktion dabei, die Schleimhaut des Magens gegen die Magensäure zu schützen.
Um Geschwüren vorzubeugen, kann der Arzt sogenannte Protonenpumpen-Hemmer verschreiben, welche die Produktion von Magensäure verringern. Eine Alternative sind Cyclooxygenase-2-Hemmer, die nur einen bestimmten Typ der Cyclooxygenase und nicht die im Magen vorkommende Version hemmen.
Weil Cyclooxygenase-Hemmer als unerwünschte Wirkung das Risiko für Herz-Kreislauferkrankungen erhöhen, sollten sie bei rheumatoider Arthritis nach Möglichkeit nicht als Dauertherapie eingesetzt werden. Auch für Rheuma-Patienten, die bereits einen Herzinfarkt erlitten haben, eignen sich diese Medikamente weniger.
Reine (nicht entzündungshemmende) Schmerzmittel (Analgetika) finden Anwendung, wenn trotz ausreichender Entzündungshemmung durch Kortikosteroide und Basistherapeutika weiterhin phasenweise oder anhaltend Schmerzen bestehen, zum Beispiel durch eingetretene Gelenkschäden. Je nach Art und Stärke der Schmerzen werden Substanzen wie zum Beispiel Paracetamol, Novaminsulfon bis hin zu Opioden (Morphin-artigen Medikamenten) verwendet.
Weitere Medikamente
Verschiedene Heilpflanzen können schmerzlindernd und entzündungshemmend wirken. Eventuell können so Schmerzmittel und Glukokortikosteroide eingespart werden.
Teufelskralle:
Die Teufelskralle ist schon seit Jahrhunderten als entzündungshemmende und schmerzlindernde Heilpflanze in Verwendung. Die Wirksamkeit bei einer rheumatoiden Arthritis ist durch Studien aber nicht eindeutig belegt. Da es einige Berichte über negative Auswirkungen wie Magen-Darm-Blutungen gibt, sollte man sich mit dem Arzt abstimmen, falls man Präparate mit Teufelskralle versuchen will.
Fischöl-Präparate:
Die Wirksamkeit von Fischöl-Präparaten beruht auf den hohen Gehalt an Omega-3-Fettsäuren. Diese Lipide reduzieren die Bildung entzündungsfördernder Sustanzen. Durch Einnahme von Fischöl kann bei der rheumatoiden Arthritis die Zahl schmerzhafter Gelenke und die morgendliche Gelenksteife vermindert werden. Eine Hemmung der Gelenkschädigung ist nicht bekannt.
Medikamente zur Injektion in das Gelenk:
Bei akuten Beschwerden kann der Arzt Kortikosteroide – gegebenenfalls mit Lokalanästhetika kombiniert – direkt in das betroffene Gelenk spritzen. Sie wirken dort rasch schmerzlindernd und entzündungshemmend.
Chemische (Chemosynoviorthese) oder radioaktive Verödungsmedikamente (Radiosynoviorthese) können ebenfalls in das betroffene Gelenk gespritzt werden, um die Gelenkinnenhaut zu veröden. Die volle Wirkung dieser Behandlung entfaltet sich erst allmählich, hält aber häufig lange an. Beide Verfahren sind jedoch noch nicht zufriedenstellend in Studien untersucht.
Operation
Eine Operation kann sinnvoll sein, wenn konservative Behandlungsmethoden nicht mehr ausreichen. Welcher operativer Eingriff zu welchem Zeitpunkt in Frage kommt, muss der Arzt im Einzelfall entscheiden. Durch die hervorragenden Möglichkeiten der medikamentösen Basistherapie sind operative Eingriffe aber erfreulicherweise immer seltener erforderlich. Prinzipiell gibt es verschiedene Möglichkeiten:
Gelenkersatz (Endoprothese):
Bei zunehmendem Verschleiß ist ein Gelenkersatz in Erwägung zu ziehen. Ziel ist es, dem Patienten wieder eine schmerzfreie oder –arme Bewegung zu ermöglichen. Zur Verfügung stehen Materialien wie Titan, Keramik, Metall oder Polyäthylen. Bei einer totalen Endoprothese werden Gelenkkopf und -pfanne ersetzt, bei einer Teilendoprothese lediglich der Gelenkkopf.
Es ist wichtig, den richtigen Zeitpunkt für einen Gelenkersatz nicht zu verpassen. Je größer der Funktionsverlust vor der Operation, desto höher ist die Wahrscheinlichkeit, dass die volle Funktionsfähigkeit auch danach nicht erreicht werden kann. Außerdem können vorgeschädigte und spröde Knochen nur eingeschränkt mechanischen Halt für die Prothese bieten.
Endoprothesen sind nur begrenzt haltbar. Zwei Operationsverfahren kommen in Frage: Bei der einen Methode wird der Prothesenschaft im Knochen einzementiert. Eine Belastung des Gelenkes ist schon nach wenigen Tagen möglich. Beim zementfreien Verfahren wird in den gesunden Knochen eine Höhle eingefräst, in die der Gelenkersatz eingesetzt wird, so dass Knochen und Prothese eine feste Verbindung eingehen können. Diese Prothesen sind meist etwas länger haltbar.
Gelenkversteifung (Arthrodese):
Dieser Eingriff erfolgt, wenn ein Gelenkersatz nicht mehr möglich ist. Die zerstörten Gelenkflächen werden entfernt und die Knochen mit Platten, Schrauben, Drähten oder Nägeln fixiert, bis das Gelenk verknöchert und versteift ist.
Gelenkresektion (Arthroplastik):
Bei zerstörten Gelenkflächen, aber noch gut erhaltenem Bandapparat, Gelenkkapsel und Muskeln wird dieser Eingriff gewählt. Nach Entfernung der zerstörten Gelenkanteile, werden die Gelenkflächen neu geformt und durch körpereigenes Gewebe (Kapselgewebe, Fettgewebe, Muskelfaszie) ersetzt. Die Gelenkresektion ist nicht für tragende Gelenke wie Hüfte oder Knie geeignet, da sie der Belastung nicht standhalten würden.
Gelenkflächenkorrektur:
Bei stärkeren Achsabweichungen wird mit der Gelenkflächenkorrektur das Ziel verfolgt, wieder eine gleichmäßige Belastung der Gelenkanteile zu erreichen beziehungsweise einen begrenzten Knorpelschaden aus der Belastungszone des Gelenks zu verlagern.
Der Knochen wird dazu durchtrennt und mittels Schrauben, Platten, Drähten und Nägeln in der korrigierten Position stabilisiert. Meist wird der Eingriff bei jüngeren Patienten durchgeführt und mit einer Synovektomie (Entfernung der Gelenkhaut) kombiniert.
Physiotherapie
Regelmäßige Physiotherapie ist ein wichtiger Baustein in der Behandlung der rheumatoiden Arthritis. Bei einer hohen Krankheitsaktivität und im akuten Schub werden die Gelenke passiv bewegt und schmerzlindernde Verfahren sowie eine schmerzarme Lagerung angewandt. Die manuelle Therapie dient der Muskellockerung. Bei einer niedrigen Krankheitsaktivität helfen aktive Bewegungsübungen die Gelenke beweglich zu halten, zu stabilisieren und Muskeln aufzubauen.
Ergotherapie
Das Ziel der Ergotherapie ist die Erhaltung oder Wiederherstellung der Selbstständigkeit. Der Patient übt in der Ergotherapie tägliche Gebrauchsfunktionen, mit dem Ziel, ein möglichst normales Leben zu führen. Er trainiert Maßnahmen für den Gelenkschutz, den Umgang mit Werkzeugen, Hilfsmitteln und Gehhilfen.
Beispiele für Alltagshilfen:
- Greifhalter: Bei eingeschränkter Bewegungsfähigkeit der Hand kommen sogenannte Greifhalter zum Einsatz. Gegenstände wie Schreibinstrumente oder Besteck können so besser gehalten werden.
- Knöpfhilfe: Das Gerät wird individuell der Handform angepasst, ist leicht zu greifen und erleichtert das Schließen von Knöpfen.
- Flaschenöffner: Zum Beispiel für Schraubverschlüsse gibt es Öffner mit speziellem Griff, die das Öffnen mit wenig Kraftaufwand ermöglichen.
Physikalische Therapie
Die physikalische Therapie hat das Ziel, die Schmerzen zu lindern und die Beweglichkeit der Gelenke möglichst lange aufrecht zu erhalten. Darüber hinaus dient sie der Muskelentspannung. Wärme- und Kältetherapie, Elektrotherapie, medizinische Bäder, Massagen oder Bewegungsbad: Für jeden Patienten gilt es, ein individuelles Therapiekonzept zusammenzustellen. Ein Verzicht auf die Basistherapie ist durch diese Maßnahmen aber nicht möglich.
Eine Kältetherapie kann zum Beispiel in Form von Bädern, Eispackungen oder einem Aufenthalt in einer Kältekammer (Ganzkörper-Kryotherapie) erfolgen. Die Schmerzrezeptoren in der Haut werden durch die Kälte kurzzeitig blockiert und so die Schmerzleitung in den Nervenfasern verringert. Gleichzeitig wirkt die Therapie abschwellend und entzündungshemmend.
Eine Wärmetherapie fördert die Durchblutung und die Muskelentspannung. Zugleich regt sie den Stoffwechsel an. Wärme kann durch Bäder, Fangopackungen, Heißluft, Rotlicht, Ultraschall oder elektrisch erzeugt werden. Bei einer akuten Gelenkentzündung ist eine Wärmebehandlung allerdings nicht sinnvoll, weil sie das entzündliche Geschehen unterstützt.
Insgesamt gilt sowohl bei Kälte- als auch Wärmeanwendungen: Nicht jedem Patienten tut dasselbe gut. Eine physikalische Therapie muss daher auf die jeweiligen Vorlieben abgestimmt sein.
Die Badetherapie (Balneotherapie) nutzt die Kombination verschiedener Physiotherapien. Kalte oder warme Bäder in verschiedenen Flüssigkeiten (Schwefelbad, Solebad) werden mit mechanischer Wirkung (Auftrieb) oder elektrischen Strömen (Stangerbad) kombiniert.
Die klassische Massage hilft gegen Muskelverspannungen. In unterschiedlichen Frequenzen hat eine Elektrotherapie unterschiedliche Wirkungsweisen. Im Nieder- und Mittelfrequenzbereich wirkt sie durchblutungsfördernd und schmerzlindernd, im Mittelfrequenzbereich auch muskelkräftigend und im Hochfrequenzbereich als Wärmetherapie eher in der Tiefe. Patienten mit Herzschrittmacher oder Metall-Implantaten (wie zum Beispiel künstlichen Gelenken) dürfen die Therapie nicht oder nur eingeschränkt anwenden.
Die Schonung eines kranken Gelenkes beschleunigt nur die Versteifung und überlastet gesunde Gelenke. Unter fachkundiger Anleitung moderat ausgeübter Sport (Schwimmen, Radfahren, Gymnastik, Spazierengehen) erhält die Beweglichkeit und kräftigt die Muskulatur. Sport in einer Gruppe macht nicht nur mehr Spaß, sondern motiviert auch gleichzeitig. Patienten mit rheumatoider Arthritis sollten sich aber immer zuerst beim Arzt beraten lassen, ob und welche Sportarten sie in welcher Intensität ausüben können.
Psychologische Therapie
Chronische Erkrankungen wie die rheumatoide Arthritis haben immer auch Auswirkungen auf die Psyche. Eine leichtere Krankheits– und Schmerzbewältigung stehen im Zentrum der psychologischen Therapie. Aber auch Entspannungstechniken, wie autogenes Training, können Rheumakranken helfen, besser mit ihrem Leiden umzugehen.
In bis zu der Hälfte der Fälle treten bei langjähriger rheumatoider Arthritis psychiatrische Erkrankungen auf: vor allem depressive Erkrankungen und Angststörungen. Diese sollten im Sinne eines ganzheitlichen Konzepts ebenso konsequent therapiert werden wie die Rheumaerkrankung selbst. So ist die Depression meist gut behandelbar; der beste Effekt wird durch Kombination von Medikamenten und regelmäßiger Psychotherapie erzielt.
Ernährung und Lifestyle
Eine spezielle Ernährung kann eine konventionelle Therapie nicht ersetzen, sie aber positiv unterstützen.
Die aufwändigen Ernährungsempfehlungen früherer Jahre im Rahmen von sogenannten "Rheumadiäten" gelten als veraltet. Günstig ist jedoch eine fleischarme Kost. Fleisch enthält nämlich große Mengen an Arachidonsäure, einem Vorläufer der entzündungsfördernden Prostaglandine. Eine kalzium- und vitaminreiche Ernährung ist wichtig, um Osteoporose vorzubeugen. Empfohlen wird heute insgesamt eine "mediterrane Kost", das bedeutet:
- mehr pflanzliches, weniger tierisches Fett
- weniger Fleisch und eher weißes, als rotes Fleisch
- mehr Fisch
- mehr Gemüse, Obst und Ballaststoffe
Daneben ist eine Reduktion von rasch resorbierbaren Kohlenhydraten sinnvoll.
Das Rauchen sollte unbedingt mit Hilfe einer professionellen Suchttherapie komplett beendet werden. Rauchen steigert die Krankheitsaktivität, mindert das Ansprechen auf die Behandlung und steigert das sowieso erhöhte Arteriosklerose-Risiko deutlich.
Alkohol kann in Maßen konsumiert werden, wobei auf die Schädlichkeit des Zellgiftes für die Leber bei gleichzeitiger Einnahme bestimmter Medikamente wie zum Beispiel Methotrexat oder Nichtsteroidale Antirheumatika besonders zu achten ist. Maximal sollten zum Beispiel von einem Mann fünf "Drinks" pro Woche getrunken werden - von einer Frau entsprechend weniger. Dabei bedeutet ein "Drink" eine kleine Flasche Bier oder ein Glas Wein (circa 12 Gramm Alkohol).
Regelmäßiges Ausdauertraining reduziert die Schmerzen, erhöht die Belastbarkeit, vermindert Müdigkeit und beeinflusst wahrscheinlich über sogenannte "Myokine" auch das Immunsystem günstig.
Die Wirkung sogenannter Radikalfänger (wie Vitamin E und C, Selen und Zink) bei einer rheumatoiden Arthritis ist wissenschaftlich nicht gesichert. Da diese Produkte auch Nebenwirkungen aufweisen, sollten Sie sich bevor Sie auf solche Mittel zurückgreifen, grundsätzlich von Ihrem Arzt oder Apotheker dazu beraten lassen!
Patientenschulung
Patientenschulungen haben zum Ziel, die Betroffenen über ihre Erkrankung aufzuklären, sie im Umgang damit zu unterstützen und praktische Hilfestellungen zu geben, die den Patienten helfen, sich auf die neue Lebenssituation einzustellen. Der Austausch mit anderen Betroffenen in Selbsthilfegruppen kann entscheidend zur Krankheitsbewältigung beitragen.

Unser Experte: Dr. Marc Schmalzing
© W&B/Privat
Beratender Experte
Dr. Marc Schmalzing ist Facharzt für Innere Medizin mit den Zusatzbezeichnungen Rheumatologie, Hämatologie und Onkologie. Seit Juli 2012 ist er als Oberarzt im Schwerpunkt Rheumatologie der Medizinischen Klinik 2 des Universitätsklinikums Würzburg tätig. Von 2008 bis 2010 war er Koordinator des interdisziplinären Rheumazentrums Tübingen (INDIRA) und von 2009 bis 2012 stellvertretender Leiter des Bereiches Rheumatologie in Tübingen.
Wichtiger Hinweis:
Dieser Artikel enthält nur allgemeine Hinweise und darf nicht zur Selbstdiagnose oder –behandlung verwendet werden. Er kann einen Arztbesuch nicht ersetzen. Die Beantwortung individueller Fragen durch unsere Experten ist leider nicht möglich.